
淺談凝聚型矽膠義乳 歷史沿革
隆乳用矽膠最初於1962年在美國推出, 1970及80年代,傳出許多起 傳統 矽膠填充物破裂、外漏案例,甚至有些婦女宣稱 傳統 矽膠滲漏遊走身體,形成硬塊,導致癌症及類風溼性關節炎等疾病。美國FDA在1992年宣布禁止使用傳統矽膠義乳植入人體 。台灣隨即跟進, 傳統 矽膠隆乳在國內正統醫療機構全面被生理食鹽水義乳取代。
雖然美國禁用十四年,但同一時間歐洲、中南美洲、亞洲部份國家並未禁用。美國接著也研發出有高聚合力、不會流動至身體其他部分的「凝聚型矽膠 (Cohesive Gel) 」 ( 即俗稱的『果凍矽膠』) 義乳。
陸續的學術研究報告也並未發現矽膠與自體免疫疾病有直接的關聯,追蹤十年後,美國食品暨藥物管理局(FDA)於2006年十一月中宣布,有條件開放使用凝聚型矽膠 (Cohesive Gel) 隆乳,但要求隆乳女性需年滿廿二歲,也要求接受凝聚型矽膠隆乳後「第三年開始,每兩年一次的乳房核磁共振檢查」,以確定沒有隱藏性滲漏發生。美國醫界甚至建議,果凍矽膠隆乳的女性應終身追蹤。

Mentor果凍矽膠義乳的特性
- 多層包裹的外殼,以減少矽膠滲漏的可能性
- 高度順滑的外層方便植入
- 嚴格的美國及歐盟標準製造規範
- 專利的(Mentor MemoryGelTM) 配方 , 給予類似乳房組織的自然觸感
Mentor果凍矽膠義乳的測試

報告結果顯示,所有測試結果皆符合美國 FDA 規定的標準與準則。
附屬研究
Mentor 公司於 1992 年 6 月開始得到美國 FDA 核准,開始進行附屬研究 /Adjunct Study 。 此研究主要針對義乳的破損、感染及莢膜攣縮做研究。截至 1998 年止,已累積超過 20,000 位患者登記參加此研究。到 2002 年,累積了 52,481 位患者、 57,684 位外科醫師登記參加此研究;共有 93,170 顆義乳被植入,有效的被調查者為 2,606 人。這份研究現正持續中。
核心研究
Mentor 公司依據美國藥物食品管制局 (FDA) 所公布的準則及與專家討論的醫材規則,要求 Mentor 公司針對該廠製造的光滑面 (smooth) 及粗糙面 (textured) 矽膠填充義乳 (Silicone Gel-filled Breast Implants) 進行為期十年的核心報告〈 Core Study 〉,以蒐集、分析此醫材的長期安全性與有效性。
此份報告指出,針對以下的症狀, Mentor 公司的矽膠義乳充分符合安全性及有效性:
隆乳:首次接受隆乳手術的婦女需年滿 20 歲。隆乳包括矯正手術。
重建:因乳癌或預防乳癌或其他病因需接受乳房組織切除手術的患者。
參加這項研究的婦女人口統計的整體基礎線是足以和參加 Mentor 的生理食鹽水義乳研究相比擬的。
關於安全性的議題,相較於使用生理食鹽水義乳患者,矽膠義乳使用患者發生併發症的比例是相似或更低於使用生理食鹽水義乳的患者。 此份 Mentor Core Gel Study 提出證據並顯示 Mentor 的矽膠義乳無害於懷孕或哺乳中的婦女。
此份報告指出,針對以下的症狀, Mentor 公司的矽膠義乳充分符合安全性及有效性:
隆乳:首次接受隆乳手術的婦女需年滿 20 歲。隆乳包括矯正手術。
重建:因乳癌或預防乳癌或其他病因需接受乳房組織切除手術的患者。
參加這項研究的婦女人口統計的整體基礎線是足以和參加 Mentor 的生理食鹽水義乳研究相比擬的。
關於安全性的議題,相較於使用生理食鹽水義乳患者,矽膠義乳使用患者發生併發症的比例是相似或更低於使用生理食鹽水義乳的患者。 此份 Mentor Core Gel Study 提出證據並顯示 Mentor 的矽膠義乳無害於懷孕或哺乳中的婦女。

完善諮詢評估,為你把關手術風險
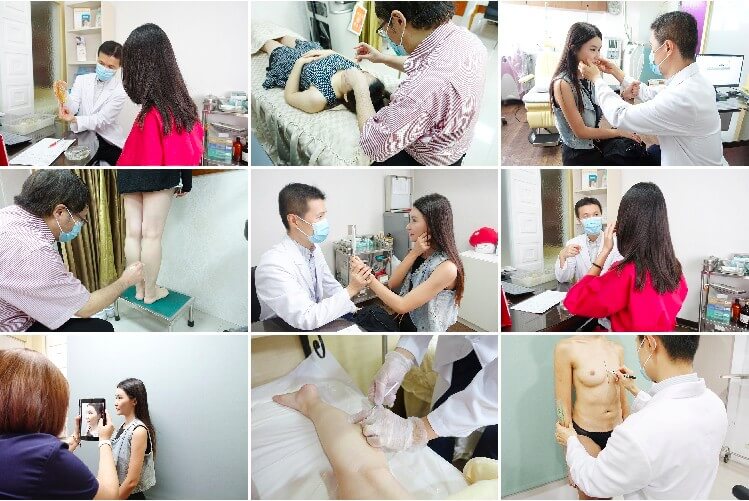
整形手術是一項過程嚴謹的工作,每位前來接受整形醫美的顧客,皆需經過醫護人員的美容需求溝通、個人健康適術評估、受術前心理評估,及醫師術前的溝通,請體諒我們在您不適合接受任何治療而給予拒絕的建議,與您取得治療前的共識是我們的堅持。整形醫美是一項追求外在更美好的事物,您的美麗請交由喬美來為您把關。
雜誌露出,整形專題報導

如果您現在有整形美容需求了,歡迎您到喬美博仕接受專業評估。
週一至週六AM09:00-PM18:00,手術諮詢請先來電預約。雷射、微整形歡迎多多利用線上LINE專人立即幫您安排預約。
諮詢專線:02-8964-5368 ,可多多利用 線上諮詢表單 來提出問題
週一至週六AM09:00-PM18:00,手術諮詢請先來電預約。雷射、微整形歡迎多多利用線上LINE專人立即幫您安排預約。
諮詢專線:02-8964-5368 ,可多多利用 線上諮詢表單 來提出問題



 為必填欄位
為必填欄位